
iNature
由于新病例的迅速增加,2019年冠狀病毒病(COVID-19)很快引起了全球關注,病原體被鑒定為SARS-CoV-2。截至目前(2021年2月10日),據約翰·霍普金斯大學發布的實時統計數據,全球累計新冠肺炎確診病例超過1億729萬例,死亡人數達234萬。這些數字每天都會更新,而且預計還會進一步增加。了解RNA病毒及其與宿主蛋白的相互作用可以改善對COVID-19的治療干預。
2021年2月9日,張強鋒,王健偉及丁強共同通訊在Cell 在線發表題為“In vivo structural characterization of the SARS-CoV-2 RNA genome identifies host proteins vulnerable to repurposed drugs”的研究論文,該研究使用icSHAPE技術,確定了SARS-CoV-2 RNA在感染的人細胞中以及從重新折疊的RNA以及SARS-CoV-2和其他六種冠狀病毒的調控性非翻譯區的結構態勢。
該研究驗證了計算機預測的幾種結構元件,并發現了影響細胞中亞基因組病毒RNA的翻譯和豐度的結構特征。結構數據提供了一種深度學習工具,可預測與SARS-CoV-2 RNA結合的42種宿主蛋白。引人注目的是,靶向結構元件的反義寡核苷酸和FDA批準的抑制SARS-CoV-2 RNA結合蛋白的藥物大大減少了SARS-CoV-2對人細胞的感染。因此,該研究的發現揭示了COVID-19治療的多種候選療法。

由于新病例的迅速增加,2019年冠狀病毒病(COVID-19)很快引起了全球關注。新型冠狀病毒感染被認為是從動物傳播的,病原體被鑒定為SARS-CoV-2。到2020年1月,懷疑最初受感染的患者是通過人與人之間的傳播感染了該病毒。
由于新病例的迅速增加,2019年冠狀病毒病(COVID-19)很快引起了全球關注,病原體被鑒定為SARS-CoV-2。截至目前(2021年2月10日),據約翰·霍普金斯大學發布的實時統計數據,全球累計新冠肺炎確診病例超過1億729萬例,死亡人數達234萬。這些數字每天都會更新,而且預計還會進一步增加。
SARS-CoV-2是冠狀病毒科的RNA病毒,該科還包括SARS-CoV,MERS-CoV。SARS-CoV-2的基因組是大約30kb的單鏈正鏈RNA,包括5'帽結構和3'poly(A)尾巴。細胞進入后,病毒基因組被翻譯成蛋白質,并且還充當復制和轉錄的模板。在翻譯過程中,SARS-CoV-2從兩個開放閱讀框(ORF1a和ORF1b)產生非結構蛋白(nsps),并從亞基因組病毒RNA產生許多結構蛋白。通過nsp12蛋白(RNA依賴性RNA聚合酶,RdRP)生成負鏈RNA,可以合成正鏈基因組RNA和亞基因組RNA。包含SARS-CoV-2基因組的RNA由亞基因組RNA編碼的結構蛋白包裝。
值得注意的是,SARS-CoV-2的大多數分子病毒學研究(以及實際上大多數其他病毒的研究)都集中在病毒蛋白上。例如,對SARS-CoV-2 S蛋白與細胞受體ACE2結合的結構測定提供了感染初始階段的原子細節。對SARS-CoV-2蛋白與人蛋白相互作用的鑒定揭示了SARS-CoV-2如何重塑細胞途徑以及被FDA批準的藥物和小分子化合物靶向的未發現的藥物宿主因子。追蹤和分析SARS-CoV-2關鍵蛋白的變化發現了一個重要的突變,與傳播增加有關。這些研究對于揭示機制的見解,以加深對分子病毒學和流行病學的了解,并有助于抗病毒療法的發展,具有重要的價值。
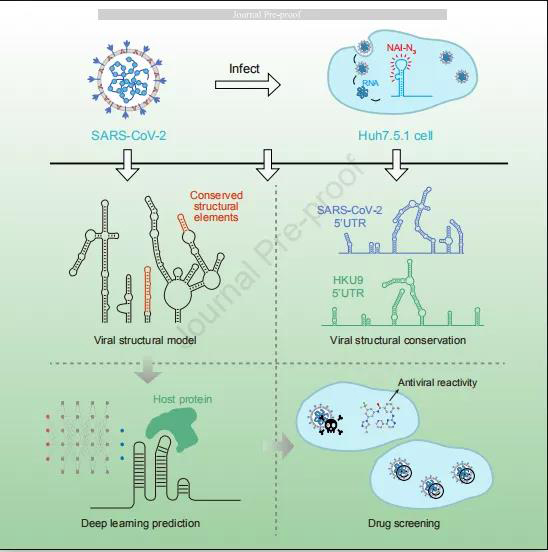
文章模式圖(圖源自Cell )
盡管如此,SARS-CoV-2是一種RNA病毒,RNA基因組本身是控制和啟用其功能的中央調節中心。RNA分子折疊成復雜的高階結構,這些結構是其細胞功能不可或缺的。在病毒中也已鑒定出許多RNA結構元件。例如,黃病毒顯示5'UTR和3'UTR之間的分子內RNA-RNA相互作用促進基因組環化并幫助協調復制;丙型肝炎病毒(HCV)5’UTR內部核糖體進入位點的結構對于翻譯至關重要;并且ZIKV和其他黃病毒的3'UTR中的多假性結結構已顯示出使RNA外切核酸酶Xrn1失速,從而產生了亞基因組黃病毒RNA,有助于病毒逃避細胞抗病毒過程。然而,盡管對SARS的幾種RNA結構元件進行了功能表征,并且最近有了關于SARS-CoV-2序列的理論預測,很明顯,對SARS-CoV-2 RNA基因組結構(存在于感染細胞中)的更全面分析對于全面了解病毒感染和治療策略至關重要。
特別令人感興趣的是,最近的一項研究發現,在Spike蛋白殘基614處帶有甘氨酸的SARS-CoV-2變異體可能具有適應性優勢。這種變體已成為該病毒的主要大流行形式。推測該氨基酸變位通過促進細胞進入或降低免疫應答來增加傳播速率。有趣的是,該變體幾乎總是伴隨SARS-CoV-2 5’UTR中的C241T突變。 不同的SARS-CoV-2株之間的結構差異也可能導致其不同的傳染性和傳播率。
更重要的是,先前對其他RNA病毒的研究已經發現了許多調節病毒感染周期的宿主RNA結合蛋白(RBP),但是這些信息SARS-CoV-2缺乏。鑒于此類相互作用對于理解病毒如何與宿主細胞相互作用至關重要,因此大規模調查和/或預測以確定感染期間哪些宿主RBP與SARS-CoV-2基因組RNA相互作用將為分子洞察提供極為豐富的資源。
該研究探討了SARS-CoV-2的體內和體外RNA二級結構,以及六種相關冠狀病毒的非翻譯區(UTRs)的結構。基于體內結構數據,該研究使用了深度學習工具來準確預測42種與SARS-CoV-2 RNA基因組的UTR結合的功能相關的宿主蛋白。該研究隨后驗證了幾種有望結合病毒RNA的蛋白質的物理和功能相互作用。
使用創新的SARS-CoV-2細胞感染系統和使用真實的SARS-CoV-2病毒進行的感染測定,該研究驗證了一些保守的RNA結構元件確實有助于病毒感染。此外,該研究發現這些宿主蛋白中的一些是易受攻擊的藥物靶標:使用經過重新定向FDA批準的藥物對它們的化學抑制作用,導致SARS-CoV-2感染細胞的明顯減少。
參考消息:https://doi.org/10.1016/j.cell.2021.02.008
轉載自“iNature”公眾號
文圖|iNature