
2021年3月9日,中國醫學科學院基礎醫學研究所劉德培團隊在Circulation上發表題為“Short-chain Enoyl-CoA Hydratase Mediates Histone Crotonylationand Contributes to Cardiac Homeostasis”的論文,研究發現Short-chain Enoyl-CoA Hydratase(ECHS1)在心臟中通過調控巴豆酰輔酶A水平維持心肌細胞穩態,首次揭示組蛋白巴豆酰化修飾在心肌肥厚等心血管疾病中發揮的病理生理作用。

我國心血管病患病率及死亡率仍處于上升階段,心血管病死亡占城鄉居民總死亡原因的首位。心肌肥厚是心臟在長期壓力負荷或容量負荷情況下發生的心臟重塑反應。在這種狀態下,伴隨著體內激素水平、分子表達、細胞結構等一系列改變,心肌細胞逐漸肥大,最終導致心功能下降,發生心力衰竭。因此,干預心臟重塑的早期心肌肥厚階段將會有效降低心衰的發生。
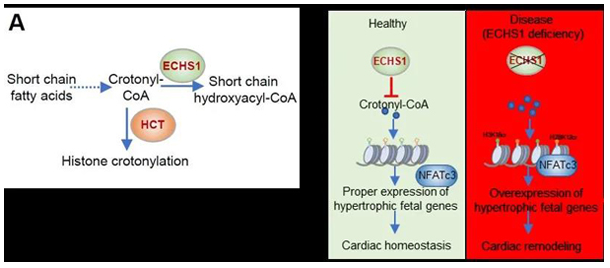
心臟是一個高耗能器官,其中70%-90%的能量來自于脂肪酸代謝,脂肪酸代謝不僅為心肌細胞提供能量,同時會產生許多代謝物(如巴豆酰輔酶A、酮戊二酸等)來修飾組蛋白,從而影響細胞的表觀遺傳和基因表達。組蛋白的表觀修飾在維持心臟穩態過程中發揮重要作用,其中組蛋白巴豆酰化(Kcr)是近年來發現的一種新型組蛋白修飾。ECHS1作為能量代謝關鍵分子SIRT3的下游參與細胞脂肪酸的β-氧化過程,其能夠水解巴豆酰輔酶A,后者可通過組蛋白巴豆酰轉移酶(HCT)的作用,參與組蛋白修飾調節。超過60%的ECHS1突變攜帶者會發生肥厚型或擴張型心肌病。
劉德培教授領導的這項研究發現ECHS1介導的組蛋白巴豆酰化修飾是臨床心肌肥厚的重要參與因素。該研究在心衰病人的心臟中發現ECHS1蛋白水平顯著降低;通過構建ECHS1基因敲除小鼠,發現ECHS1純合敲除小鼠發生胚胎死亡,雜合缺陷小鼠在血管緊張素II的刺激下顯著促進心肌肥厚發生,相反心肌細胞特異性過表達ECHS1則能夠保護心肌肥厚發生。通過RNA-seq等高通量測序和生信分析以及實驗研究,他們發現ECHS1缺陷增強組蛋白H3K18cr和H2BK12cr修飾,促進NFATC3轉錄因子在心肌肥厚基因啟動子上募集,促進心肌肥厚和心臟重塑的發生。該研究解釋了人群ECHS1突變導致心臟缺陷的病理機制,提出調節組蛋白巴豆酰化是治療心肌肥厚及心衰的新策略,具有重要的臨床意義。
本研究得到了國家重點研發項目(2019YFA0801500, 2020YFC2008003)、中國醫學科學院醫學與健康科技創新工程(2017-I2M-1-008)、中國醫學科學院中央級公益性科研院所基本科研業務費(2019-RC-HL-006)、國家自然科學基金(91849207, 82030017, 81800273, 81970426)等項目的資助。基礎醫學研究所劉德培課題組博士畢業生唐小強(現為四川大學副研究員)和陳小鳳(現為成都中醫藥大學講師)及2018級直博生孫鑫為該論文的共同第一作者,劉德培教授和陳厚早教授為共同通訊作者。這也是繼此團隊2017年在該雜志發現能量限制介導分子SIRT2對抗老年心肌肥厚和心臟重塑后的又一力作(具體見:Circulation 2017 Nov 21;136(21):2051-2067;https://pubmed.ncbi.nlm.nih.gov/28947430/ 和微信公眾號“衰老與抗衰老”:https://mp.weixin.qq.com/s/MjdsvgG39uwl-WAe-SOXEw)。
論文鏈接:https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.120.049438
文圖| 基礎醫學研究所